納米銀的殺菌原理是什么?
信息來源: http://sharewhatyouteach.com 時間:2018-11-8 15:34:26
納米銀(silver nanoparticle.SNP)具有高效廣譜、不易產生抗藥性、安全性高的優點,是當前抗菌材料研究的熱點。但現在對SNP抗菌劑里的認識仍有不同觀點,進一步深入的研究仍在繼續。
在日常生活中應用銀作為抗菌材料的例子有很多。如皮膚受傷時,醫護人員會使用銀絲織成的紗布包扎皮膚創傷;用銀制的容器盛放食物可以延長食物的保質期等等。20世紀30年代科學家發現了抗生素后,由于抗生素的廣泛使用導致銀系抗菌材料被人們忽視。近年來,由于抗生素的濫用導致細菌產生抗藥性問題嚴重,所以,以SNP為代表的新型低成本安全性高的抗菌材料又引起的人們的關注。
SNP作為抗菌材料具有許多優良的特性。
首先,SNP的安全性高。相比于銀離子,SNP在濃度極低(納摩爾或微摩爾)時就對微生物表現出強烈的抗菌性,而對哺乳動物的毒性較低并且很少出現并發癥。
其次,持久性好。SNP可以負載于殼聚糖等載體上,持續釋放出零價銀離子,維系較為穩定的銀濃度,達到持久抗菌的目的。
第三,廣譜抗菌。SNP能夠有效抑制包括金黃色釀膿菌、葡萄球菌、大腸桿菌、綠膿假單胞菌等多種致病菌,以及皮膚癬菌等真菌在內的650多種致病菌,甚至可以殺死HIV-1。
第四,不易產生耐藥性。經SNP處理的細菌基本無法存活,可以杜絕細菌產生耐藥性。
第五,SNP還有毒副作用小,使用方便等優點。
但是,納米作為抗菌材料使用時也暴露出一些問題,例如銀累積和遷移造成的生活和安全問題。銀富集到較高濃度時對人體和哺乳動物有較大危害,會隨呼吸進入線粒體、胚胎以及肝臟和循環系統等。有研究指出SNP比鋁和金等金屬的納米顆粒毒性更強,因此SNP在作為抗菌材料應用的范圍和使用劑量也值得研究和關注。
目前SNP研究機理尚不充分,通常認為是SNP釋放銀離子發揮作用并誘導產生活性氧(ROS)。另有研究發現SNP本身直接發揮抗菌作用并協同釋放的銀離子發揮作用。現階段普遍認同的SNP的抗菌原理主要有影響細菌生活的環境、破壞細胞壁、抑制DNA復制、抑制酶呼吸作用、抑制其他酶活性等。
SNP通過影響細菌的生活環境發揮抗菌作用。
在溶液中,受氧氣和質子協同作用,SNP釋放出銀離子或被氧氣氧化形成納米氧化銀再釋放銀離子,發揮抗菌作用。
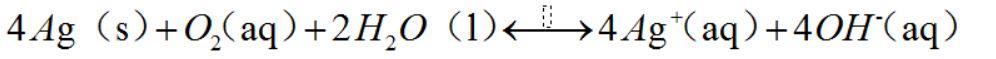
有研究認為,SNP本身對細菌無影響,抑制作用源于釋放銀離子且嚴格依賴氧氣濃度。
在有氧條件下SNP和氧化銀顆粒都表現出較強的抗菌性。但細菌有氧呼吸等新陳代謝極大降低了氧氣的含量,導致銀離子濃度降低并失去抗菌能力。而環境中氧氣濃度下降對需氧細菌的影響巨大,直接抑制甚至殺死細菌。
此外,銀離子可與體系中營養元素結合,降低細菌生長所必須的元素濃度。
也要研究表明,SNP誘導氧氣產生氧離子,水分子產生羥基,加劇消耗氧氣的同時,對細胞膜進行攻擊。在較高濃度銀離子下,銀離子可重新聚集成零價銀離子,因此該過程不斷持續消耗氧氣并發揮抑菌作用。
SNP通過破壞細胞壁發揮抗菌作用。
銀離子和SNP負載正電荷通過與帶有負電荷的菌體蛋白質之間的靜電吸引,吸附在細胞膜上。因其較高的表面能和分散性,SNP與細胞壁之間發生化學作用并破壞細胞壁的完整性。在細胞壁富集電子部位表現尤為明顯。導致細胞壁正常功能如營養滲透等喪失。
同時,SNP和銀離子作為膜的過氧化誘導劑,與部分蛋白和磷酸脂質作用,誘導膜損傷或分解。
有研究報道指出粒徑小于20納米的SNP易于含硫蛋白結合,干擾蛋白功能并引起細胞壁滲透性變大。說明滲透性改變是抗菌的重要途徑。
SNP通過抑制DNA復制發揮抗菌作用。
SNP通過膜蛋白和脂質作用(包括滲透性改變和穿孔等)突破細胞壁進入細菌體內。SNP進入菌體內聚集形成低分子量的聚集體,細胞壁與細胞膜分離,使DNA為免受SNP的破壞而聚集濃縮。導致DNA停留在復制間期而無法完成復制過程。或者通過阻斷細菌內的電子傳輸系統增強細菌DNA的穩定性,DNA無法解開雙螺旋,失去復制能力,細菌分裂速度下降。
SNP和銀離子通過與含大量供電子原子的細胞核、擬核和線粒體的DNA結合,抑制DNA復制甚至喪失復制能力。
SNP通過抑制酶呼吸作用發揮抗菌作用。
許多研究認為SNP抑制細菌呼吸作用是另一種抑菌方式,途徑包括降低菌體內外氧氣濃度,直接作用于呼吸和ATP生成相關酶。
SNP溶解釋放銀離子過程消耗氧氣,而氧氣在細菌環境和菌體內的溶解度降低,有效抑制了細菌呼吸。
SNP通過抑制其他酶的活性發揮抗菌作用。
SNP進入細胞,因靜電吸引,首先與胞內負載有負電荷的酶、蛋白質組或者細胞器和脂質結合。進而與酶中的硫、氧和氫等電子供體(L-半胱氨酸等)結合,甚至替換酶中金屬離子,致使酶活性鈍化甚至失活。在創傷輔料中,SNP通過抑制基質金屬蛋白酶抑制其生長因子的降解作用,提高創傷愈合速度。
此外,銀離子和SNP與功能蛋白中的氨基酸殘基(半胱氨酸硫基)、氨基、咪唑、磷酸和羧基等親核性集團結合,改變酶三維構象,導致蛋白不可逆變性,細菌正常代謝無法進行。
而革蘭氏陰性菌中,SNP作用于磷酸酪氨酸多肽,觀察到磷酸酪氨酸去磷酸化,而蛋白質的磷酸化過程與細菌體內的信號傳導有關,據此推斷SNP通過影響菌體的信號傳導,從而抑制或者中斷細菌的生長。
綜上所述,SNP在溶液中部分溶解釋放出銀離子,SNP和銀離子錨定在細菌細胞壁上帶有負電荷的功能團上,功能蛋白受銀的作用,細菌細胞壁和細胞膜結構發生變化,功能紊亂,尤其是改變了膜的滲透性,進入細胞質,同時引起細菌營養元素的流失。銀在細胞質中損壞DNA結構抑制其復制以及呼吸鏈酶等相關活性,最終導致細菌失活。但是在實際環境中由于氧氣的存在,SNP變化涉及到復雜的生化過程,包括SNP的聚集、銀離子的釋放、銀離子與有機物等絡合、以及溶解沉淀平衡等,SNP抑菌過程仍有待進一步研究。
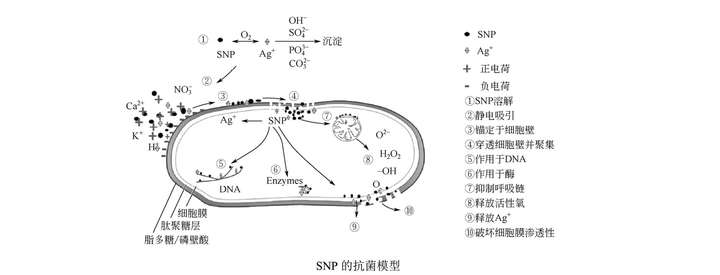
參考文獻:【1】吳宗山.納米銀的抗菌機理研究進展【J】.化工進展,2015,(34):1349-1355.
 微信
微信



